教授 浜本洋Hiroshi HAMAMOTO, Ph.D.
所属学会
American Society for Microbiology
日本化学療法学会
日本細菌学会
日本医真菌学会
日本薬学会
学会活動
Drug Discovery and Therapeutics誌, Associate Editor
Journal of Antibiotics (Tokyo), Editorial Board
公的委員
ナショナルバイオリソースプロジェクト(カイコ)運営委員
日本医療開発機構 AMED課題評価委員 (2021年度-2023年度)
教育専門分野
微生物学、全身疾患学
研究テーマ
1. ライソシンEの作用機序の解析・実用化研究
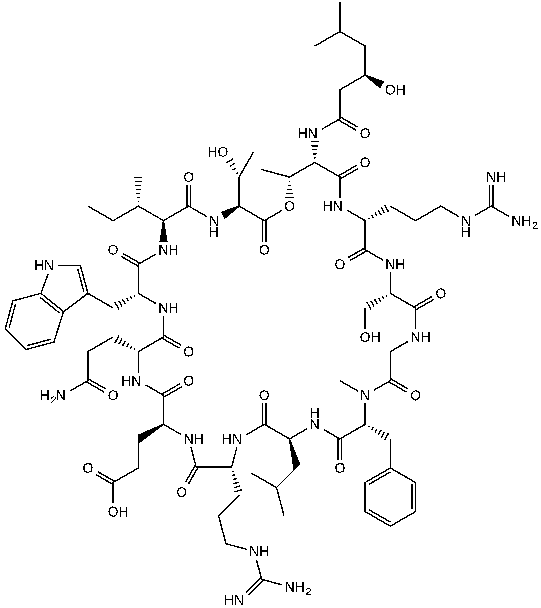 ライソシンEの開発研究を進めています。
これは沖縄の土壌から分離した菌が生産する抗生物質であり、難治性MRSAの治療薬として有望です。
この研究では、カイコ黄色ブドウ球菌感染モデルを用いた治療効果の評価に基づいて、ライソシンEの探索を行いました(業績14)。
ライソシンEは非常にユニークな作用機序を持っており、血清中のアポリポプロテインA-IとIIによって抗菌活性が上昇し、高い治療効果を示すことがわかっています(業績3)。
さらに、ライソシンEは黄色ブドウ球菌の殺菌活性において、他の抗MRSA薬よりも優れた効果を示し、わずか1分で99.9%以上の殺菌率を実現します。
この強力な殺菌活性のメカニズムを解明するための研究を進めています。
また、臨床試験のためのライソシンEの開発研究も行っています。
ライソシンEの開発研究を進めています。
これは沖縄の土壌から分離した菌が生産する抗生物質であり、難治性MRSAの治療薬として有望です。
この研究では、カイコ黄色ブドウ球菌感染モデルを用いた治療効果の評価に基づいて、ライソシンEの探索を行いました(業績14)。
ライソシンEは非常にユニークな作用機序を持っており、血清中のアポリポプロテインA-IとIIによって抗菌活性が上昇し、高い治療効果を示すことがわかっています(業績3)。
さらに、ライソシンEは黄色ブドウ球菌の殺菌活性において、他の抗MRSA薬よりも優れた効果を示し、わずか1分で99.9%以上の殺菌率を実現します。
この強力な殺菌活性のメカニズムを解明するための研究を進めています。
また、臨床試験のためのライソシンEの開発研究も行っています。
また、薬剤耐性菌に対抗するためには、ライソシンEだけでは不十分です。新しい抗生物質の発見とその作用機序の解析に取り組んでいます。 特許関連の事情から詳細は明かせませんが、この研究は抗薬剤耐性菌に対する戦略に大きく貢献することを期待しています。
2. 細菌・真菌の病原性発揮機構の解析
細菌・真菌は、宿主環境下でどのようにして病原性を発揮するのかを明らかにするため、次世代シーケンサーによる網羅的な発現解析を行っています(業績2)。 この取り組みにより、従来の常識からは異なる現象も明らかになってきました。 また、網羅的遺伝子破壊株ライブラリーを用いて、カイコ感染モデルにおいて病原性が低下する株を見つけ出し、新たな病原性発現機構の解明も進めています(業績5, 7)。 これらの研究では、試験管内での増殖には関与しないが、病原性に関連する代謝機構を標的とした創薬開発に取り組んでいます。
連絡先
E-mail: hamamoto★med.id.yamagata-u.ac.jp
※「★」を「@」にご変換ください
主な業績
すべての業績はリサーチマップ もしくはGoogle Scholarを参照
1. Geberetsadik G, Inaizumi A, Nishiyama A, Yamaguchi T, Hamamoto H, Panthee S, Tamaru A, Hayatsu M, Mizutani Y, Kaboso S A, Hakamata M, Ilinov A, Ozeki Y, Tateishi Y, Sekimizu K, Matsumoto S: Lysocin E Targeting Menaquinone in the Membrane of Mycobacterium tuberculosis Is a Promising Lead Compound for Antituberculosis Drugs, Antimicrob Agents Chemother, 66, e0017122, 2022
2. Hamamoto H, Panthee S, Paudel A, Ohgi S, Suzuki Y, Makimura K, Sekimizu K: Transcriptome change of Staphylococcus aureus in infected mouse liver, Commun Biol, 5, 721, 2022
3. Hamamoto H, Panthee S, Paudel A, Ishii K, Yasukawa J, Su J, Miyashita A, Itoh H, Tokumoto K, Inoue M, Sekimizu K: Serum apolipoprotein A-I potentiates the therapeutic efficacy of lysocin E against Staphylococcus aureus, Nat Commun, 12, 6364, 2021
4. Panthee S, Hamamoto H, Nishiyama Y, Paudel A, Sekimizu K: Novel pathogenic mucorales identified using the silkworm infection model, J Fungi (Basel), 7, 995, 2021
5. Paudel A, Panthee S, Hamamoto H, Grunert T, Sekimizu K: YjbH regulates virulence genes expression and oxidative stress resistance in Staphylococcus aureus, Virulence, 12, 470-480, 2021
6. Panthee S, Paudel A, Hamamoto H, Uhlemann A C, Sekimizu K: The role of amino acid substitution in HepT toward menaquinone isoprenoid chain length definition and lysocin E sensitivity in Staphylococcus aureus, Front Microbiol, 11, 2076, 2020
7. Paudel A, Hamamoto H, Panthee S, Matsumoto Y, Sekimizu K: Large-scale screening and identification of novel pathogenic Staphylococcus aureus genes using a silkworm infection model, J Infect Dis, 221, 1795-1804, 2020
8. Takada Y, Itoh H, Paudel A, Panthee S, Hamamoto H, Sekimizu K, Inoue M: Discovery of gramicidin A analogues with altered activities by multidimensional screening of a one-bead-one-compound library, Nat Commun, 11, 4935, 2020
9. Itoh H, Tokumoto K, Kaji T, Paudel A, Panthee S, Hamamoto H, Sekimizu K, Inoue M: Development of a high-throughput strategy for discovery of potent analogues of antibiotic lysocin E, Nat Commun, 10, 2992, 2019
10. Panthee S, Paudel A, Hamamoto H, Sekimizu K: Complete genome sequence of Weissella hellenica 0916-4-2 and its comparative genomic analysis, Front Microbiol, 10, 1619, 2019
11. Panthee S, Paudel A, Hamamoto H, Sekimizu K: Advantages of the silkworm as an animal model for developing novel antimicrobial agents, Front Microbiol, 8, 373, 2017
12. Paudel A, Hamamoto H, Panthee S, Kaneko K, Matsunaga S, Kanai M, Suzuki Y, Sekimizu K: A novel spiro-heterocyclic compound identified by the silkworm infection model inhibits transcription in Staphylococcus aureus, Front Microbiol, 8, 712, 2017
13. Kaji T, Murai M, Itoh H, Yasukawa J, Hamamoto H, Sekimizu K, Inoue M: Total synthesis and functional evaluation of fourteen derivatives of lysocin E: importance of cationic, hydrophobic, and aromatic moieties for antibacterial activity, Chem Eur J, 22, 16912-16919, 2016
14. Hamamoto H, Urai M, Ishii K, Yasukawa J, Paudel A, Murai M, Kaji T, Kuranaga T, Hamase K, Katsu T, Su J, Adachi T, Uchida R, Tomoda H, Yamada M, Souma M, Kurihara H, Inoue M, Sekimizu K: Lysocin E is a new antibiotic that targets menaquinone in the bacterial membrane, Nat Chem Biol, 11, 127-133, 2015
15. Murai M, Kaji T, Kuranaga T, Hamamoto H, Sekimizu K, Inoue M: Total synthesis and biological evaluation of the antibiotic lysocin e and its enantiomeric, epimeric, and N-demethylated analogues, Angew Chem Int Ed Engl, 54, 1556-1560, 2015
16. Ishii K, Adachi T, Hamamoto H, Sekimizu K: Serratia marcescens suppresses host cellular immunity via the production of an adhesion-inhibitory factor against immunosurveillance cells, J Biol Chem, 289, 5876-5888, 2014
17. Ishii K, Adachi T, Imamura K, Takano S, Usui K, Suzuki K, Hamamoto H, Watanabe T, Sekimizu K: Serratia marcescens induces apoptotic cell death in host immune cells via a lipopolysaccharide- and flagella-dependent mechanism, J Biol Chem, 287, 36582-36592, 2012
18. Ishii K, Hamamoto H, Imamura K, Adachi T, Shoji M, Nakayama K, Sekimizu K: Porphyromonas gingivalis peptidoglycans induce excessive activation of the innate immune system in silkworm larvae, J Biol Chem, 285, 33338-33347, 2010
19. Ishii K, Hamamoto H, Kamimura M, Nakamura Y, Noda H, Imamura K, Mita K, Sekimizu K: Insect cytokine paralytic peptide (PP) induces cellular and humoral immune responses in the silkworm Bombyx mori, J Biol Chem, 285, 28635-28642, 2010
20. Kurokawa K, Hamamoto H, Matsuo M, Nishida S, Yamane N, Lee B L, Murakami K, Maki H, Sekimizu K: Evaluation of target specificity of antibacterial agents using Staphylococcus aureus ddlA mutants and D-cycloserine in a silkworm infection model, Antimicrob Agents Chemother, 53, 4025-4027, 2009
21. Ishii K, Hamamoto H, Kamimura M, Sekimizu K: Activation of the silkworm cytokine by bacterial and fungal cell wall components via a reactive oxygen species-triggered mechanism, J Biol Chem, 283, 2185-2191, 2008
22. Orihara Y, Hamamoto H, Kasuga H, Shimada T, Kawaguchi Y, Sekimizu K: A silkworm baculovirus model for assessing the therapeutic effects of antiviral compounds: characterization and application to the isolation of antivirals from traditional medicines, J Gen Virol, 89, 188-194, 2008
23. Hamamoto H, Kamura K, Razanajatovo I M, Murakami K, Santa T, Sekimizu K: Effects of molecular mass and hydrophobicity on transport rates through non-specific pathways of the silkworm larva midgut, Int J Antimicrob Agents, 26, 38-42, 2005
24. Hamamoto H, Kurokawa K, Kaito C, Kamura K, Manitra Razanajatovo I, Kusuhara H, Santa T, Sekimizu K: Quantitative evaluation of the therapeutic effects of antibiotics using silkworms infected with human pathogenic microorganisms, Antimicrob Agents Chemother, 48, 774-779, 2004
25. Akimitsu N, Hamamoto H, Inoue R, Shoji M, Akamine A, Takemori K, Hamasaki N, Sekimizu K: Increase in resistance of methicillin-resistant Staphylococcus aureus to beta-lactams caused by mutations conferring resistance to benzalkonium chloride, a disinfectant widely used in hospitals, Antimicrob Agents Chemother, 43, 3042-3043, 1999
